Binnen de ontwikkeling van nieuwe medicijnen speelt onderzoek met behulp van proefpersonen een grote rol. Het succes van klinisch onderzoek is afhankelijk van de vrijwillige deelname van patiënten aan zulke medische onderzoeken. Daar is Novartis deze patiënten zeer dankbaar voor. We proberen patiënten zo vroeg mogelijk in de opzet van onze studies te betrekken en ondersteunen onze onderzoekers bij het juist informeren van hun potentiële kandidaten.
Door mee te doen aan klinisch onderzoek helpen patiënten niet alleen mee aan het ontwikkelen van nieuwe geneesmiddelen voor toekomstige patiënten met dezelfde ziekte. Ze krijgen zelf ook eerder toegang tot nieuwe behandelmogelijkheden, al voordat deze op de markt zijn. Daarmee biedt meedoen aan klinisch onderzoek soms een extra optie tot behandelen als er niets anders meer mogelijk is.
Patiënten kunnen veel vragen hebben over deelname aan medisch-wetenschappelijk onderzoek. Op deze pagina staat toegankelijke informatie over het belang van wetenschappelijk onderzoek en hoe het precies in zijn werk gaat. Zo kan iedereen een goed geïnformeerde keuze maken over eventuele deelname aan klinisch onderzoek van Novartis.
Waarom meedoen aan medisch-wetenschappelijk onderzoek van Novartis?
Medisch-wetenschappelijk onderzoek verschilt van “gewoon” medisch onderzoek. Wanneer een patiënt naar de dokter gaat voor een onderzoek omdat hij of zij medische klachten heeft, noemt men dat medisch onderzoek. Medisch-wetenschappelijk onderzoek is wetenschappelijk onderzoek waarbij het onderzoek gericht is op het ontwikkelen van nieuwe kennis, medicijnen of technieken. Dit wordt ook wel klinisch onderzoek genoemd.
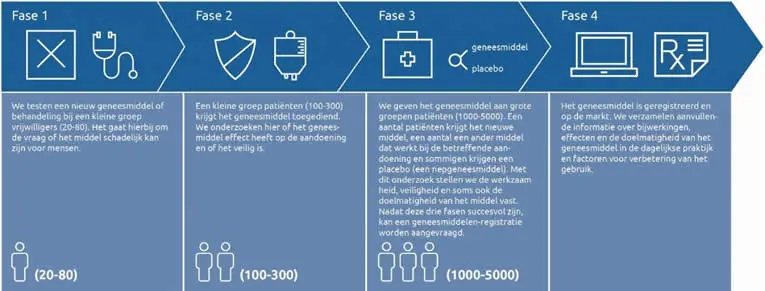
Tijdens klinisch onderzoek wordt het potentiële geneesmiddel getest bij mensen. Het middel is dan al getest op proefdieren en veilig bevonden. Klinisch onderzoek gebeurt in 4 fases. Ook tijdens de klinische onderzoeken kan een potentieel medicijn nog altijd afvallen als het niet naar verwachting werkt. Het klinische onderzoeksproces neemt gemiddeld zo’n 6 jaar in beslag en moet voldoen aan de strenge eisen die gelden voor wetenschappelijk onderzoek.