MAYO 13, 2026
Dra. Marina Alonso / Dr. Fernando Caravaca
Descripción de la patología
La glomerulonefritis membranoproliferativa mediada por inmunocomplejos (GNMP-IC) no es una enfermedad renal per se, sino que representa un patrón histológico de daño renal como resultado de diversas etiologías18. Este patrón debe motivar la búsqueda de una causa subyacente, aunque en un porcentaje variable de casos no se logra determinarla con exactitud, estableciéndose el término de GNMP-IC primaria. Las principales etiologías incluyen enfermedades autoinmunes sistémicas (lupus eritematoso sistémico, síndrome de Sjögren...), infecciones (hepatitis B, C, fúngicas o parasitarias), crioglobulinemia y paraproteinemias19. Se ha descrito que en algunas formas de GNMP-IC primaria la desregulación del complemento podría jugar un papel fundamental y, por tanto, podrían considerarse en el mismo espectro patogénico que la glomerulopatía C3 (GC3)20.
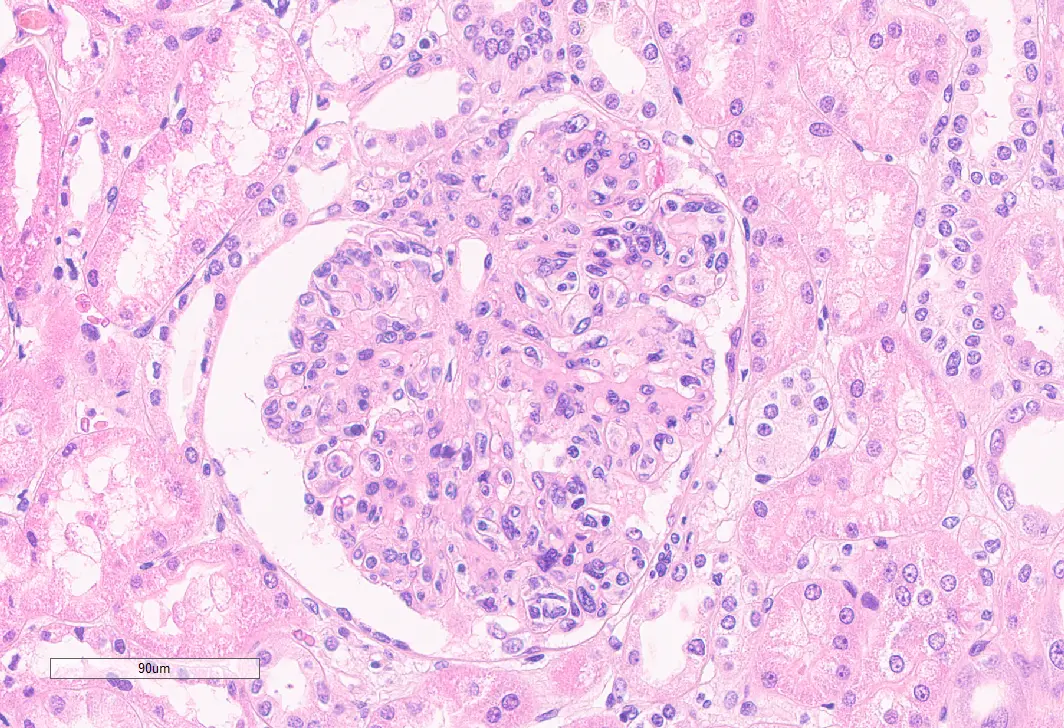
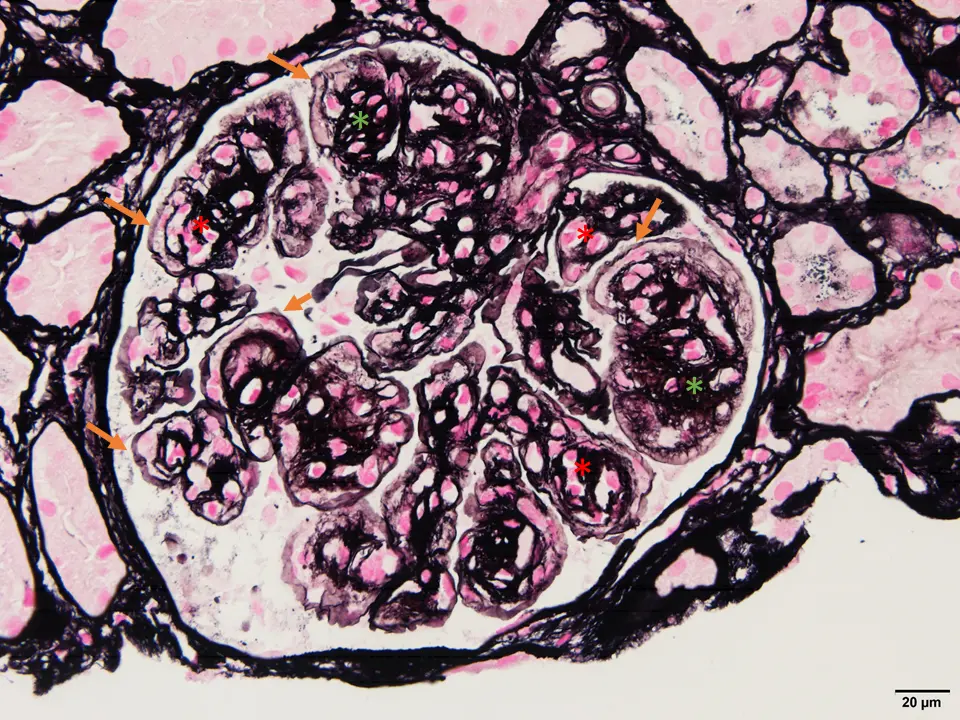
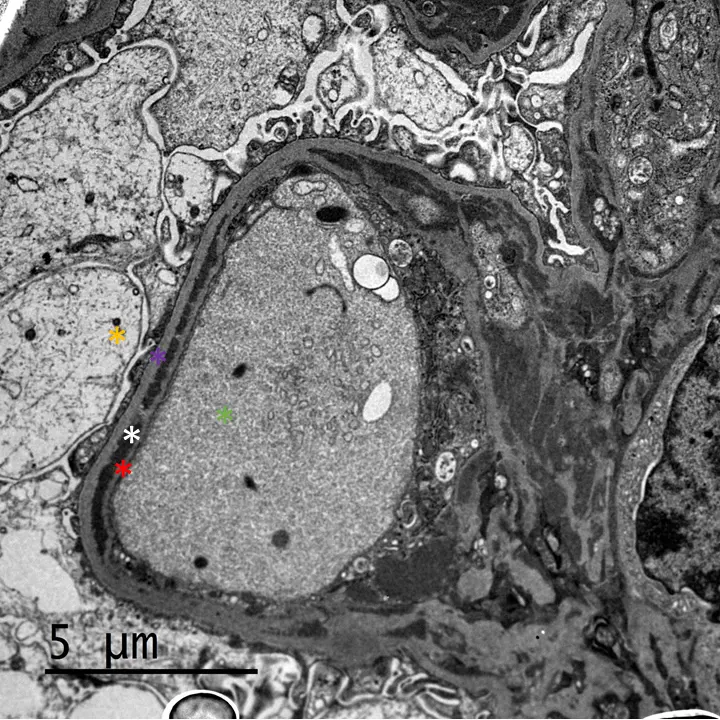
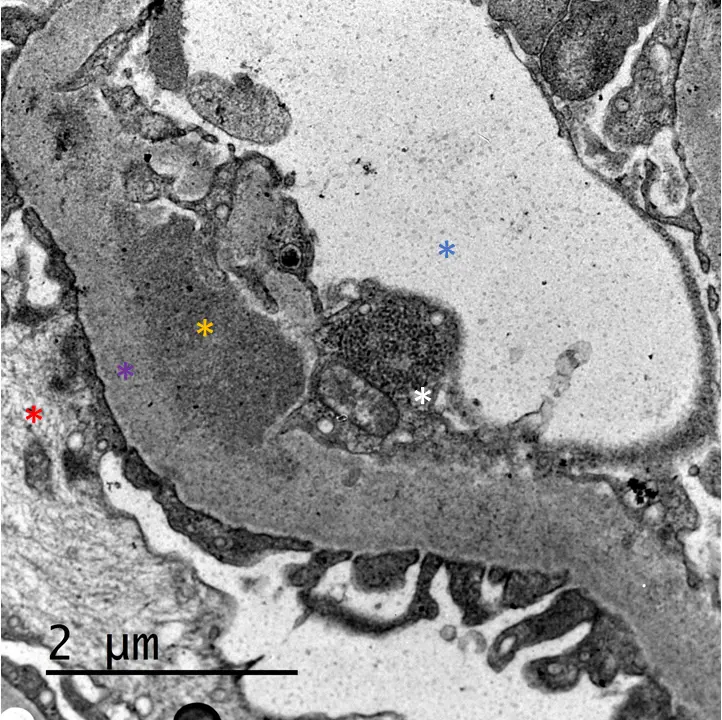
Histológicamente, presenta un patrón caracterizado por hipercelularidad endocapilar y mesangial, y engrosamiento de las paredes capilares que puede acompañarse de dobles contornos en la plata (Imgs. 1 y 2)21.
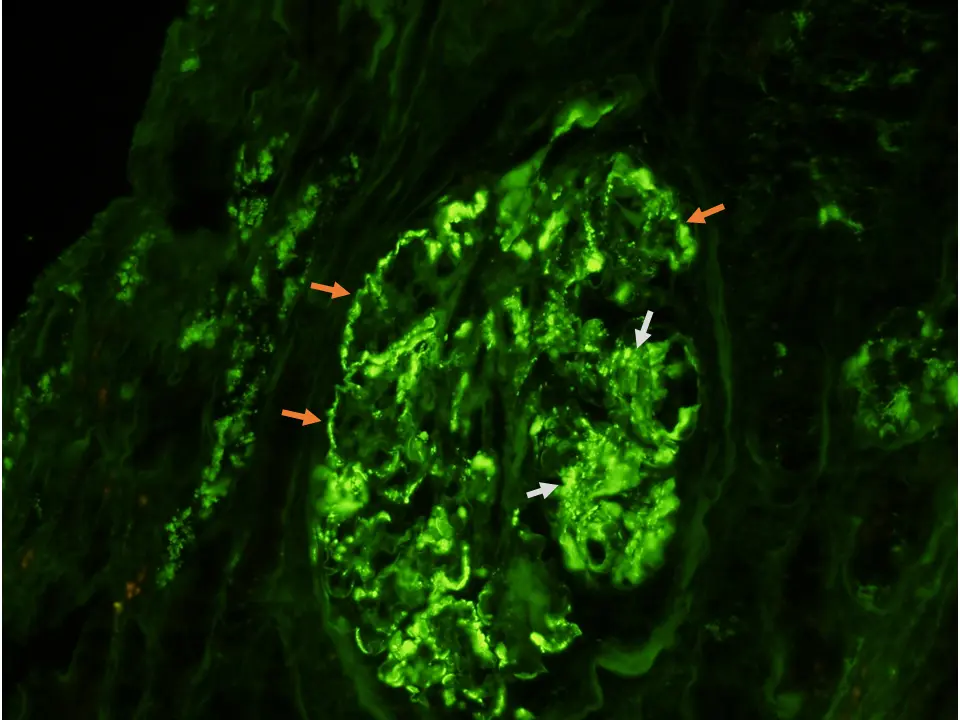
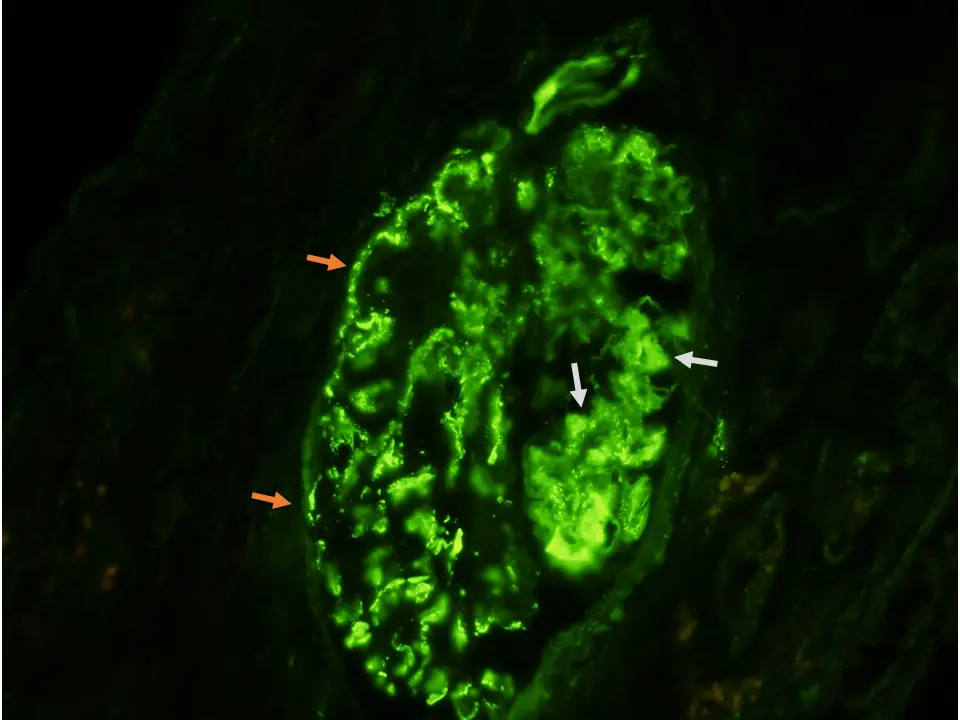
La inmunofluorescencia directa (IFD) muestra depósitos mesangiales y parietales de inmunoglobulinas (Ig) policlonales, acompañados de complemento, con igual o mayor intensidad de tinción de Ig frente a C3 (Imgs. 3 y 4). Los depósitos parietales suelen ser de aspecto pseudolineal grosero; si se asocian depósitos subepiteliales puede verse un patrón más granular22. Mediante microscopía electrónica (ME), los depósitos son electrodensos no estructurados de localización subendotelial (antigua GNMP tipo I) (Img. 5), o van acompañados por depósitos subepiteliales o intramembranosos (antigua GNMP tipo III). La imagen ultraestructural es inespecífica, aunque algunas lesiones en IFD (depósitos vasculares o tubulares) o ME (inclusiones túbulo-reticulares en las células endoteliales, depósitos «en huella dactilar») pueden orientar hacia la etiología en algunos casos (Img. 6)21.
Presentaciones más frecuentes
Puede diagnosticarse tanto en niños como en adultos. La presentación clínica es similar a la descrita en la GC3, predominando proteinuria no nefrótica con microhematuria y función renal conservada, o síndrome nefrótico completo23,24.
Un 50% de los casos de GNMP-IC primaria pueden presentar hipocomplementemia C3, y se ha descrito la misma prevalencia de variantes patogénicas en genes del complemento o anticuerpos C3Nef 25.
Las manifestaciones clínicas también dependerán de la etiología subyacente, apareciendo signos de infección en casos con infecciones asociadas, o manifestaciones de las enfermedades autoinmunes sistémicas responsables.
Se ha descrito la transformación de GNMP-IC inicial en una GC3 en una biopsia renal posterior. Aunque no está plenamente demostrado, se postula que estos casos son en realidad GC3 con depósitos transitorios de inmunoglobulinas en el seno de procesos infecciosos intercurrentes26.
Puntos clave para el diagnóstico diferencial
Clínicos
- La presentación clínica es similar a la de la GC3.
- Es preciso buscar una posible etiología subyacente, incluyendo serologías virales, estudio de autoinmunidad del complemento (incluyendo ANA, anti-DNA), espectro electroforético, inmunofijación y cadenas ligeras libres en suero. De esta manera podríamos descartar una posible etiología autoinmune sistémica (p. ej., lupus) o una gammapatía monoclonal.
- A diferencia de la GNMP-IC secundaria, la frecuencia de C4 sérico bajo (activación de vía clásica) es muy baja en la GNMP-IC primaria (<3 %).
- Hasta la fecha, no hay indicios de que la respuesta al tratamiento disponible sea diferente en la GNMP-IC y la GC3.
Histológicos
- El patrón histológico más frecuente es el de glomerulonefritis membranoproliferativa.
- El depósito de Ig, evidenciado por IFD, suele tener la misma intensidad y distribución que el depósito de complemento; la diferencia entre ambos debe ser de menos de 2+ de intensidad
- Las Ig que más frecuentemente se depositan son IgG e IgM.
- El depósito de complemento mayoritario suele ser C3, aunque pueden verse otros factores (C4, C1q).
- Ambas cadenas ligeras kappa y lambda deben ser positivas.